Endometriosis
From imaging to clinical diagnosis
Publié le 01 Sep 2020Lecture 10 min
Intérêt de l’IRM pelvienne dans le diagnostic et la prise en charge de l’endométriose
Mikhael BENJOAR, Centre d’imagerie Manin Crimée, Paris ; Hôpital Tenon, Paris
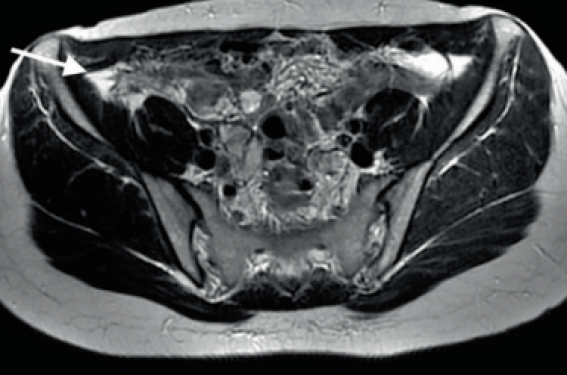
Cet article a pour but de résumer l’intérêt de l’IRM dans le diagnostic, le suivi et la cartographie préopératoire de l’endométriose. Nous abordons ici les éléments techniques nécessaires et suffisants pour un diagnostic précis, ainsi que les éléments sémiologiques de base pour la bonne reconnaissance de la pathologie.
L’endométriose se définit par la présence de tissu endométrial en dehors de la cavité endométriale comportant à la fois des glandes et du stroma. Cette pathologie est fréquente, touchant 10 % des femmes en âge de procréer. Le délai moyen entre le début de la symptomatologie et un diagnostic établi reste long, proche des 8 ans. Les symptômes principaux sont les dysménorrhées, les dyspareunies et l’infertilité. L’endométriose est aujourd’hui un problème de santé publique majeur ; le ministère de la Santé a mis en place une campagne d’information nationale.
Indications
Une IRM pelvienne doit être précédée d’une échographie gynécologique. Elle permet une recherche simple et performante d’endométriomes qui apparaissent comme des formations kystiques avec un fin piqueté échogène homogène. La recherche d’une endométriose profonde est beaucoup plus complexe et nécessite d’être menée par un échographiste expert. L’IRM pourra être proposée chez des patientes avec atteinte clinique ou avec une endométriose visualisée en échographie (ovarienne simple ou endométriose profonde). Elle peut être aussi proposée en cas d’échographie négative chez des patientes avec forte suspicion clinique (dyspareunie ou dysménorrhées intenses).
Techniques
L’IRM est un examen bien toléré et non invasif. Une claustrophobie importante reste un obstacle. Un jeûne de 4 heures et nécessaire. Un lavement rectal 2 h avant l’examen est systématiquement prescrit pour permettre une analyse performante de la paroi recto-sigmoïdienne. La réalisation d’une opacification rectale ou vaginale au gel d’échographie n’a pas montré sa supériorité en termes de performance diagnostique ; il n’est donc pas recommandé de la réaliser. L’injection intraveineuse de gadolinium n’a pas non plus montré de supériorité(1). Seule une injection sous-cutanée d’antipéristaltique type glucagon est réalisée 10 minutes avant l’examen. L’analyse repose sur les séquences T2 sans saturation de graisse. Des études récentes ont montré l’intérêt des nouvelles séquences 3D T2 permettant un reformatage dans tous les plans de l’espace(2). Les séquences T1 sans et avec saturation de la graisse permettent la recherche et la caractérisation des implants hémorragiques (endométriomes et implants superficiels). L’interprétation doit être réalisée par un radiologue expert.
Endométriose ovarienne
Les endométriomes sont une localisation fréquente d’endométriose, ils sont facilement identifiables en IRM sur les séquences T1. Ils apparaissent en hyper signal T1 supérieur à la graisse sur la séquence T1 sans saturation de graisse (figure 1a) ; cet hypersignal persiste après la suppression de signal graisseux (figure 1b). En T2, l’endométriome se caractérise par un « shading » c’est-à-dire une chute de signal variable, qui peut aller d’un discret hyposignal T2 à un vide de signal complet (figure 1c). Les endométriomes sont souvent bilatéraux et multiples. L’atteinte tubaire va se caractériser par des hématosalpinx endométriosiques qui sont des formations tubulées présentant des caractéristiques de signal semblables aux endométriomes. La différenciation entre endométriomes et hématosalpinx est souvent difficile mais indispensable dans le cadre des prises en charge en PMA. L’IRM permet une mesure optimale de ces endométriomes ainsi qu’une évaluation de la fonction ovarienne résiduelle. Elle va permettre de détecter d’éventuelles complications des endométriomes : la dégénérescence et la surinfection.
Figure 1 : Aspect typique d’un endométriome ovarien gauche. A. Hypersignal T1 spontané supérieur à la graisse. B. Persistance de l’hypersignal T1 après saturation de la graisse. C. Hyposignal T2 modéré en rapport avec un "shading".
• Une dégénérescence sera évoquée sur la présence d’un porion tissulaire apparaissant en hyposignal T1, signal T2 intermédiaire, hypersignal de diffusion et se rehaussant après injection. Les formes histologiques fréquentes sont des lésions épithéliales endométrioïdes ou des lésions à cellules claires.
• Une surinfection d’endométriomes sera recherchée dans un contexte infectieux évident : les abcès vont perdre leur signal endométriosique, présenter un hypersignal T1 modéré, un hyposignal T2 périphérique et un rehaussement pariétal extrêmement important (figure 2). L’IRM permet une cartographie optimale et la planification d’un drainage chirurgical ou radiologique.
Figure 2 : Aspect de surinfecion d’un endométriome ovarien gauche. A. Hyposignal T1 avec présence d’une bulle d’air déclive. B. Hyposignal T2 périphérique de la coque de l’abcès. C. Rehaussement intense après injection de la coque de l’abcès.
Endométriose sous-péritonéale postérieure
L’IRM est très performante pour la détection et la cartographie précise des lésions d’endométriose profonde. Elle se caractérise par la présence de fibrose rétractile qui se manifeste elle-même par un franc hyposignal T2 et T1. La présence de spots en hypersignal T1 FAT SAT correspond à des implants hémorragiques d’endométriose superficielle surajoutée. La localisation la plus fréquente se situe sur les ligaments utérosacrés et le torus uterinum. Ces structures anatomiques sont des moyens de fixation de l’utérus à la paroi pelvienne. Les ligaments utérosacrés rejoignent à leurs porions distales les lames sacro-rectogénito-pubiennes. Le torus uterinum correspond à la jonction de ces deux ligaments en arrière de la jonction isthme/col utérin. Néanmoins, la localisation du torus est variable en hauteur. À l’état normal, ces structures peuvent être visualisées ; elles apparaissent comme deux structures linéaires et fines en hyposignal T2. Leur visualisation est facilitée par la présence d’un épanchement libre dans le cul-de-sac de Douglas. Une atteinte sera affirmée par un épaississement focal supérieur à 3 mm d’épaisseur, la présence de spicules ou d’implants hémorragiques. La recherche de cette atteinte est facilitée par la réalisation d’une séquence spécifique en T2 en coupes fines à haute résolution de 3 mm d’épaisseur parallèle au plan de ces ligaments(3). La sensibilité et la spécificité sont évaluées respectivement à 84 et 89 %, supérieures à celles de l’échographie endo-vaginale et de l’écho-endoscopie rectale(4). L’aspect classique est celui de « moustache rétro-cervicale » avec la visualisation, juste en arrière du col, d’un épaississement spiculé du torus et de l’origine des deux ligaments utéro-sacrés (figure 3).
Figure 3 : Exemples d’épaississement du torus et des ligaments utérosacrés chez 3 patientes différentes (flèches blanches).
Cette atteinte fibrosante s’accompagne fréquemment d’un phénomène rétractile avec attraction des ovaires en arrière et phénomène de « kissing ovaries » (figure 4d). L’atteinte va potentiellement s’étendre vers l’arrière et vers la charnière sigmoïdienne. Différents types d’atteinte sont possibles allant de la simple adhérence à une atteinte de la musculeuse digestive, voire de la sous-muqueuse.
L’atteinte digestive sera affirmée en IRM par la présence de nodule en franc hyposignal T2 dans la musculeuse digestive. La sensibilité et la spécificité sont respectivement évaluées à 87 % et 93 %(4) ; dans la littérature, ces performances sont inférieures à celles de l’échographie endovaginale et équivalentes à celles de l’écho-endoscopie rectale (figure 4). La réalisation d’un lavement, préalable à l’IRM, permet de mieux analyser la paroi digestive. L’utilisation des séquences 3D permet une bonne évaluation et représentation dans l’espace de ces atteintes. Le compte rendu radiologique devra indiquer la présence ou non de cette atteinte digestive, la distance entre le pôle inférieur de la lésion et la marge anale, la longueur et l’épaisseur de l’atteinte. Les nouvelles techniques de résection chirurgicale discoïdes nécessitent une évaluation de l’atteinte dans le plan axial du recto-sigmoïde, laquelle ne devrait pas s’étendre sur plus de 25 % de la circonférence recto-sigmoïdienne. L’IRM permet aussi de détecter les lésions recto-sigmoïdiennes multifocales, notamment en cas de dolichosigmoïde avec une deuxième atteinte en regard de la fossette ovarienne gauche.
Figure 4 : Atteinte digestive en T2 chez deux patientes différentes. A. Atteinte extensive en coupes sagittales T2 avec atteinte allant jusqu’à la sous-muqueuse (flèches blanches). B. Atteinte extensive en coupes axiales T2 avec atteinte allant jusqu’à la sous-muqueuse (flèches blanches). C. Atteinte limitée à la musculeuse en hyposignal T2 en coupes sagittales T2 (flèches blanches). D. Atteinte limitée à la musculeuse en hyposignal T2 en coupes axiales T2 (flèches blanches) avec aspect de "kissing ovaries".
L’atteinte peut aussi s’étendre vers le bas en atteignant le cul-de-sac vaginal postérieur ; son identification en imagerie est difficile, alors que son évaluation clinique est aisée. En IRM, cette atteinte va se caractériser par un épaississement du cul-de-sac vaginal postérieur en hyposignal T2 (figure 5a et c) et par la présence de spots hémorragiques en hypersignal T1 après saturation de la graisse (figure 5b et d). La sensibilité et la spécificité sont évaluées à 85 % et 72 %, beaucoup plus élevées que celles de l’échographie endo-vaginale et de l’écho-endoscopie rectale(4). Toutes ces lésions peuvent être associées et réaliser une symphyse complète du cul-de-sac de Douglas avec un accolement complet du sigmoïde à la face postérieure de l’utérus (figure 4d).
Figure 5 : Exemples d’atteinte du cul-de-sac vaginal postérieur. A. Atteinte spiculée du cul-de-sac vaginal postérieur en T2 coupes fines (flèche blanche). B. Implant hémorragique visible en sagittales T1 après saturation de la graisse en regard du cul-de-sac vaginal postérieur (flèche blanche). C. Atteinte kystique du cul-de-sac vaginal postérieur en T2 coupes fines (flèche blanche). D. Implant hémorragique visible en sagittales T1 après saturation de la graisse en regard du cul-de-sac vaginal postérieur (flèche blanche).
Endométriose sous-péritonéale antérieure
Les localisations antérieures sont plus rares (5 à 10 %), définies par une infiltration du cul-de-sac vésico-utérin avec une atteinte plus ou moins importante de la paroi vésicale. Elles seront affirmées par la présence de nodules en hyposignal T2 dans cette paroi (figure 6a et b). Les atteintes antérieures sont fréquemment le siège d’implants hémorragiques en hypersignal T1 (figure 6c). L’importance et le degré d’infiltration de la paroi vésicale devront être bien décrits pour planifier un geste chirurgical adéquat.
Figure 6 : Atteinte centrée sur le cul-de-sac vésico-utérin. A. Nodule spiculé centré sur le cul-de-sac vésico-utérin en coupes axiales T2 (flèche noire). B. Nodule spiculé centré sur le cul-de-sac vésico-utérin en coupes sagittales T2 (flèche blanche). C. Nodule hémorragique avec implants en hypersignaux T1 avec saturation de la graisse (flèche blanche).
Endométriose latérale
Les atteintes extensives d’endométriose vont s’étendre aux paramètres et aux parois pelviennes latérales. Ces atteintes latérales vont se compliquer fréquemment de lésions urétérales pouvant entraîner une dilatation des cavités pyélocalicielles(5). C’est pour cette raison que toute IRM doit comporter une exploration rénale. Les lésions peuvent aussi atteindre l’insertion des ligaments ronds sur les cornes utérines et s’étendre jusqu’au canal de Nuck par ces ligaments (figure 7).
Figure 7 : Atteinte antérolatérale centrée sur le ligament rond droit et s’étendant au canal de Nuck. A. Coupe axiale T2 montrant un nodule en regard de l’insertion du ligament rond sur la corne utérine droite (flèche blanche) et un nodule en hyposignal T2 en regard du canal de Nuck dans la paroi abdominale (flèche creuse). B. Implants hémorragiques en T1 avec saturation de la graisse en regard de la corne utérine droite (flèche blanche).
Formes rares
D’autres atteintes plus rares et plus difficiles à explorer peuvent bénéficier d’une IRM, telle l’atteinte du bas-fond cæcal et de la dernière anse iléale (figure 8). L’atteinte de la paroi abdominale antérieure peut donner des aspects de pseudo-tumeur des paries molles avec des masses spiculées en franc hyposignal T2 pouvant être le siège d’implants hémorragiques. L’atteinte diaphragmatique ne sera recherchée qu’en cas de douleurs cataméniales de l’hypochondre droit ou en cas d’antécédents de pneumothorax cataménial. La visualisation d’implants hémorragiques diaphragmatiques permet d’affirmer le diagnostic.
Figure 8 : Atteinte du bas fond cécal chez une patiente présentant une endométriose digestive multifocale. A. Atteinte spiculée en coupes axiales T2 (flèche blanche). B. Implants hémorragiques en hypersignaux T1 avec saturation de la graisse (flèche blanche).
Conclusion
L’IRM est aujourd’hui un outil incontournable du diagnostic et du bilan d’extension de la maladie endométriosique. Elle permet au clinicien d’évaluer avec précision les localisations et l’extension de la maladie afin de déterminer avec précision le traitement optimal, chirurgical ou médical, pour soulager au mieux les patientes en termes de douleurs, de qualité de vie ou de fertilité.
Attention, pour des raisons réglementaires ce site est réservé aux professionnels de santé.
pour voir la suite, inscrivez-vous gratuitement.
Si vous êtes déjà inscrit,
connectez vous :
Si vous n'êtes pas encore inscrit au site,
inscrivez-vous gratuitement :